
Васенина Елена Евгеньевна, д.м.н., доцент кафедры неврологии с курсом рефлексологии и мануальной терапии ФГБОУ ДПО РМАНПО
[embedded content]
Современные эпидемиологические исследования показывают, что женщины значительно чаще, чем мужчины, страдают от тревожных и депрессивных расстройств, как эндогенных, так и вторичных [1,2].
Например, частота тревоги и депрессии среди женщин в 2-3 чаще, чем среди мужчин [3]. Вместе с этим течение аффективных расстройств у женщин отличается более выраженными симптомами, тяжестью и длительностью, худшим ответом на терапию, склонностью к рецидивам и менее благоприятным прогнозом. В то же время мужчины чаще демонстрируют лучший клинический ответ на лечение: у них быстрее купируются острые эпизоды, а дальнейшее течение заболевания оказывается более стабильным. Одним из возможных факторов, влияющих на эти различия, могут быть половые гормоны. Их роль в развитии и особенностях течения аффективных расстройств до конца не изучена, однако предполагается, что гормональные колебания у женщин (например, во время менструального цикла, беременности или менопаузы) могут повышать риск возникновения аффективных симптомов. Это открывает новые направления для исследований, которые помогут лучше понять природу этих расстройств и разработать более эффективные методы лечения с учетом гендерных особенностей.«Женское лицо» тревоги
Гендерные различия в предрасположенности к аффективным расстройствам, в частности к тревоге и депрессии, можно объяснить через два ключевых механизма. С одной стороны, мужские половые гормоны играют роль «защитного» фактора, снижающего риск развития аффективных нарушений.
С другой стороны, женские половые гормоны, напротив, формируют повышенную предрасположенность к возникновению тревожно-депрессивных расстройств. В этом контексте тестостерон, основной мужской половой гормон, оказывает наиболее выраженное защитное действие. Это подтверждается рядом исследований. Например, мужчины с гипогонадизмом значительно чаще страдали от различных вариантов аффективных нарушений. Аналогично, применение андроген-подавляющей терапии при лечении рака предстательной железы увеличивало риск развития тревожных расстройств. Это значит, что снижение уровня тестостерона делало мужчин более уязвимыми к аффективным нарушениям. Заместительная терапия тестостероном, напротив, была эффективна в купировании тревожных симптомов как у мужчин, так и у женщин. Связь между уровнем тестостерона и тревожными расстройствами наблюдается и у женщин: у пациенток с диагностированными тревожными расстройствами отмечается обратная корреляция между риском развития тревоги и уровнем тестостерона.Так почему аффективные расстройства имеют «женское лицо»? Ключевыми факторами, которые делают женщин более уязвимыми к развитию аффективных расстройств, являются изначально более низкий уровень тестостерона (в 10 раз ниже, чем у мужчин) и его возрастное снижение, а также женские половые гормоны, такие как эстроген и прогестерон, и гормональные колебания, характерные для женского организма. Вместе низкий уровень тестостерона в сочетании с влиянием женских половых гормонов создают уникальный «гормональный фон», который предрасполагает женщин к развитию тревоги и депрессии. Таким образом, аффективные расстройства действительно имеют «женское лицо» — они чаще встречаются у женщин, протекают тяжелее и требуют особого подхода в диагностике и лечении.
Почему женщины более уязвимы к развитию тревоги? Пять причин
Причина 1. Стрессоустойчивость и реактивность
Женщины более склонны к развитию тревожных расстройств, чем мужчины, и одна из основных причин этого кроется в их физиологической реактивности на стресс. Мужчины, как правило, более стрессоустойчивы, в то время как женщины демонстрируют более выраженные и избыточные стрессовые реакции на физиологическом уровне. Это различие во многом связано с работой мозга, особенно с активностью миндалины – структуры, которая играет центральную роль в формировании эмоционального и стрессового ответа.
Миндалина – ключевой элемент системы реагирования на опасность. Она активируется в ответ на угрозу, и, воздействуя на вегетативные центры и базальные ганглии, запускает каскад быстрых, рефлекторных физиологических реакций («драться или убегать»), таких как учащение сердцебиения, повышение давления и выброс гормонов стресса. Однако у здоровых людей префронтальная кора и передняя поясная кора подавляют избыточную активность миндалины, обеспечивая нисходящий контроль над эмоциями. Это позволяет человеку регулировать свои реакции и не поддаваться панике. У пациентов с генерализованным тревожным расстройством этот механизм нарушен. Исследования с использованием функциональной магнитно-резонансной томографии показывают, что у таких пациентов наблюдается гипоактивация корковых областей, в частности префронтальной и передней поясной коры, что приводит к дефициту контроля над миндалиной. В результате миндалина продолжает находиться в гиперактивированном состоянии, что проявляется в виде постоянной тревоги и чрезмерных стрессовых реакций [4].
Миндалина регулируется активностью ГАМК-ергических рецепторов. Гамма-аминомасляная кислота (ГАМК) — это главный тормозной нейротрансмиттер центральной нервной системы. Чем выше активность ГАМК, тем меньше возбудимость миндалины и, соответственно, ниже уровень тревоги и риск затяжных длительных стрессовых ответов. Именно на этом принципе, усилении эффектов ГАМК посредством агонизма ГАМК-ергических рецепторов и последующем снижении активности миндалины, основано действие многих анксиолитических препаратов, таких как бензодиазепины. Однако у женщин стрессовые реакции часто оказываются более затяжными, что может быть связано с менее эффективной ГАМК-ергической регуляцией. Это делает их более уязвимыми к развитию тревожных расстройств.
Тестостерон играет важную роль в регуляции уровня ГАМК и ГАМК-ергической нейротрансмиссии за счет своих активных метаболитов. Одни из конечных продуктов метаболизма тестостерона, андростан-3α,17β-диолы, хотя и не действуют как классические половые гормоны (имеют низкое сродство к андрогеновым рецепторам), обладают высоким сродством к ГАМК-ергическим рецепторам (Рис. 1). Выступая в роли нейростероидов, они модулируют активность ГАМК, сдерживая и подавляя возбудимость миндалины и снижая стрессовые реакции. Так мужчины получают большую стрессоустойчивость.
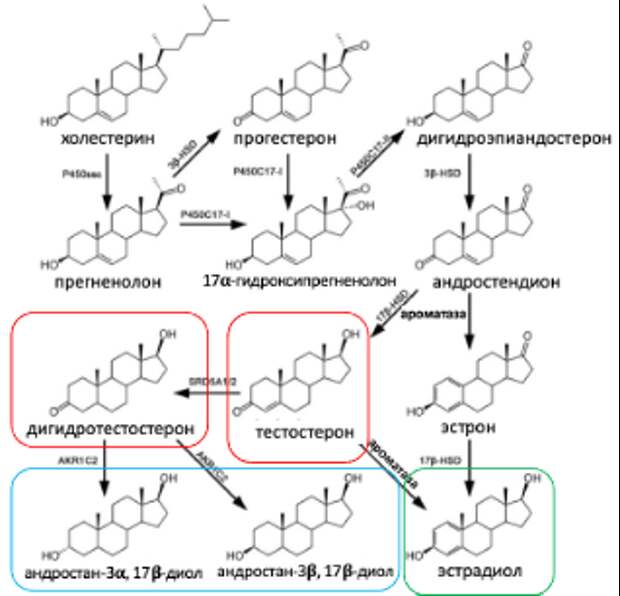
Рисунок 1. Схематичное изображение метаболизма половых гормонов.
У женщин уровень тестостерона изначально в 10 раз ниже, чем у мужчин, что может объяснять их большую уязвимость к любым эмоциональным переживаниям и, соответственно, более высокий риск развития тревожных расстройств. Кроме того, с возрастом уровень тестостерона у женщин снижается еще больше, что дополнительно повышает их уязвимость. Исследования показывают, что у женщин с диагностированными тревожными расстройствами наблюдается обратная корреляция между уровнем тестостерона и выраженностью тревоги: чем ниже уровень тестостерона, тем выше риск развития тревоги.
Причина 2. Система вознаграждения
Мужчины и женщины имеют тонкие различия в строении и работе головного мозга, которые обуславливают их эмоциональное восприятие и поведение. В частности, у мужчин более активно работает система вознаграждения и удовольствия, что позволяет им лучше воспринимать положительные эмоции. В то же время женщины, на физиологическом уровне, больше фиксированы на негативных переживаниях. Говоря о структурных различиях, под воздействием половых гормонов у женщин более активно развивается преоптическая область гипоталамуса, которая является ключевой зоной материнского инстинкта. У мужчин же более активно развивается прилежащее ядро – центр системы вознаграждения. Система вознаграждения, или система внутреннего подкрепления, представляет собой совокупность структур нервной системы, которые участвуют в регулировании и контроле поведения на основании положительных эмоций и действий. Благодаря этой системе, действия, поступки и решения закрепляются положительными эмоциями: в присутствии удовольствия и какой-то пользы от результата поведение и цель встраиваются в автобиографическую память, чтобы в дальнейшем использоваться для выработки оптимальной модели поведения при столкновении с подобной ситуацией в будущем. Ключевым нейромедиатором в этой системе является дофамин – истинный «гормон удовольствия».
Ключевую роль в регуляции поведения играет лимбическая система. Структуры лимбической системы формируют два уровня эмоционального реагирования. Миндалина участвует в формировании поведения на основе отрицательных эмоций, способствуя реализации стратегии избегания, тогда как гиппокамп отвечает за регуляцию поведения на основе положительных эмоций, закрепляя поведение достижения через получение удовольствия (Рис. 2).
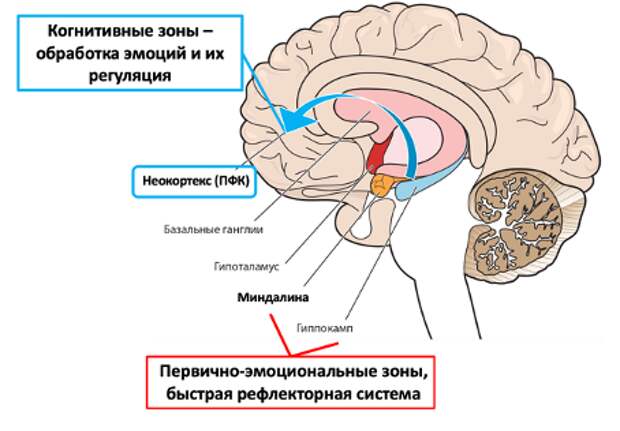
Рисунок 2. Структуры коры и лимбической системы головного мозга, участвующие в регуляции эмоционального реагирования. ПФК, префронтальная кора.
Исследования показывают, что мужчины и женщины по-разному реагируют на получение удовольствия от результата. В животных моделях in vivo было показано, что введение тестостерона в лимбические структуры у мужчин оказывало противотревожный и антидепрессивный эффекты, тогда как эстрогены, наоборот, потенцировали тревожное и депрессивное поведение [5]. В целом, мужчины более ориентированы на получение удовольствия и вознаграждения, что позволяет им проще получать удовольствие от результата. Женщины же чаще ориентируются на избегание негативных результатов, а также меньше получают удовольствие от итогового результата.
Наконец, на уровень тревоги современного человека в целом и женщины в частности немаловажное влияние оказывает социальное равенство. С одной стороны, оно подразумевает равные возможности и права для всех, независимо от пола, расы, возраста и т.п. Но есть и обратная сторона: женщины сталкиваются с дополнительными стрессовыми факторами, связанными с необходимостью балансировать между карьерой и семьей. Помимо этого, эволюционно женщины менее склонны к рискам и болезненно переживают неудачи, так как чувствительнее к отрицательным эмоциям. Сложности с получением удовольствия от результата приводят к перфекционизму и неспособности остановиться.
Причина 3. Нарушения сна
Первичные эмоциональные реакции человека играют важную роль в его поведении и восприятии окружающего мира. Они включают оценку реальности угрозы, адекватности поведения и принятых решений, соответствия эмоциональных реакций, предшествующего опыта, риска повторения и других факторов. В то время как миндалина воспринимает опасность и обеспечивает быструю рефлекторную реакцию, когнитивная оценка и обработка стрессового эпизода структурами неокортекса и гиппокампом, в свою очередь, играют ключевую роль в выработке оптимальной модели поведения, позволяя избежать «неоправданных рефлекторных» действий (в том числе через регуляцию эмоций). Повторные стрессогенные ситуации требуют не только анализа, но и подавления рефлекторного эмоционального/стрессового ответа и корректировки ранее сформированных поведенческих паттернов. Именно когнитивный контроль в данном случае становится ключевым механизмом, позволяющим адаптировать поведенческий ответ под социальные условия и нормы и избежать неадекватных стрессовых реакций.
Обработка полученного опыта информации происходит ночью, в медленно-волновой фазе сна. В этой связи нарушения сна часто влекут за собой дефицит контроля и обработки эмоций, что, в свою очередь, способствует развитию тревожных и депрессивных расстройств. Таким образом, нарушения сна – еще одна причина более высокой распространенности тревожных и депрессивных расстройств у женщин.
Причина 4. Прогнозирование опасности
Другая причина более высокой частоты тревожных расстройств у женщин – склонность к избыточному прогнозированию опасности. В отличие от мужчин, женщины более склонны ожидать потенциальных угроз, анализировать возможные риски и пытаться избежать опасности. Такое поведение, хотя и может быть полезным в некоторых ситуациях, в долгосрочной перспективе становится фактором риска развития тревоги. Источники этих различий кроются как в биологических, так и поведенческих факторах – особенностях работы мозга, социальных установках и биологических различиях между полами.
У женщин лобная кора, которая играет важнейшую роль в регуляции эмоций и стрессовых реакций, активно вовлечена в процесс прогнозирования. Она отвечает за анализ информации, обработку данных, сопоставление текущей ситуации с предыдущим опытом, оценку адекватности реакций, выработку оптимального поведения и, наконец, прогнозирование возможных угроз. У женщин эта область мозга работает более интенсивно, что делает их более склонными к постоянному анализу потенциальных опасностей. Однако такая склонность к избыточному прогнозированию может приводить к катастрофизации и нагнетанию обстановки, особенно в условиях неопределенности. Постоянные попытки избежать опасности и ожидание худшего способны инициировать тревожные переживания и запускать стрессовые реакции даже в отсутствие реальной угрозы.
Социальные и биологические факторы также усиливают эту склонность. Женщины часто воспитываются в условиях, где их учат быть более осторожными и предусмотрительными, что формирует привычку к постоянному прогнозированию. На плечи современной женщины также ложится много ответственности за близких, что только увеличивает количество поводов для переживаний. Наконец, гендерные различия в нейрохимическом функционировании мозга также играют немаловажную роль. У мужчин активность серотонина и дофамина – нейротрансмиттеров, связанных с чувством удовлетворения и устойчивостью к стрессу, – обычно выше, что делает их менее склонными к «негативному» вектору восприятия. У женщин, напротив, более низкая активность этих систем может усиливать тревожные переживания и склонность к избыточному прогнозированию. Постоянное ожидание опасности и попытки избежать угрозы создают порочный круг. Женщины, склонные к избыточному прогнозированию, чаще испытывают стресс, даже когда реальной опасности нет. Это приводит к хронической активации и дезадаптации стрессовых систем организма, что, в свою очередь, повышает риск развития тревожных расстройств. Со временем такие переживания могут стать привычными, формируя устойчивый паттерн тревожного поведения.
Таким образом, склонность женщин к избыточному прогнозированию опасности – это сложный феномен, который объединяет особенности работы мозга, социальные установки и биологические различия. Лобная кора, отвечающая за анализ и прогнозирование, у женщин работает более интенсивно, что делает их более уязвимыми к тревоге. В сочетании с повышенной ответственностью за близких и меньшей активностью серотониновой и дофаминовой систем это создает благоприятные условия для развития тревожных расстройств. Понимание этих механизмов помогает не только объяснить, почему женщины чаще страдают от тревоги, но и сформировать пути для более эффективной помощи, учитывающей индивидуальные особенности пациентов.
Причина 5. Обработка эмоциональной травмы и посттравматическое стрессовое расстройство
Женщины более уязвимы к развитию посттравматического стрессового расстройства (ПТСР), чем мужчины, и это связано с особенностями их восприятия и обработки эмоциональной травмы и реакций на стресс. Когда женщина сталкивается с ситуацией, которая воспринимается как чрезвычайно опасная и угрожающая жизни, ее мозг, посредством активации вегетативных центров, «превентивно» активирует механизмы, направленные на избегание повторения подобного опыта. Это приводит к тому, что мельчайшие детали травмирующего события – запахи, звуки, визуальные образы – запоминаются с особой интенсивностью. Такая «гипермнезия» позволяет женщине быть «наготове» при малейшем намеке на возможный повтор угрожающей ситуации. Однако эта особенность также становится основой для развития ПТСР.
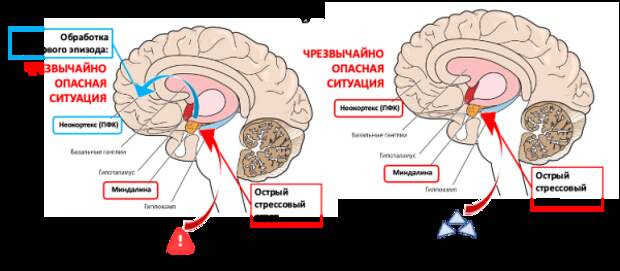
Второй сценарий формирования ПТСР – это гиперсенсибилизация к опасности. В данном случае даже минимальные, незначимые стимулы, которые могут напоминать о травмирующем событии, способны инициировать развернутый стрессовый ответ. Поскольку эти реакции направлены на обеспечение выживания, они не осознаются и не подвергаются глубокой когнитивной обработке, а реализуются рефлекторно. Это связано с тем, что женщины в целом более склонны к стрессовым реакциям и характеризуются меньшей стрессоустойчивостью. Одной из причин этого является более низкая активность ГАМК-ергической системы – главного регулятора миндалины, которая отвечает за формирование страха и тревоги. У женщин менее эффективная работа этой системы делает их более восприимчивыми к стрессу и менее способными быстро восстанавливаться после эмоциональных потрясений (Рис. 3).
Рисунок 3. Механизм формирования ПТСР: гиперсенсибилизация к опасности. Гипереактивность или гиперсенсибилизация неокортекса после перенесения жизнеугрожающей стрессовой ситуации (А) приводит к инициации развернутого стрессового ответа в ответ на незначимые стимулы (Б).
Кроме того, как упоминалось выше, у женщин менее развита «система вознаграждения», которая отвечает за получение положительных эмоций и удовольствия. Это означает, что они менее ориентированы на поиск радости и удовлетворения в своих действиях и поведении. Вместо этого для женщин более типичен перфекционизм: они часто менее удовлетворены итоговым результатом своих усилий и сложнее останавливаются на достигнутом. Такая установка создает дополнительное напряжение и повышает риск развития тревожных расстройств, включая ПТСР.
Как и в случае с тревожными расстройствами в целом, нарушения сна являются еще одним фактором, способствующим развитию ПТСР у женщин. Женщины более подвержены риску развития инсомнии, при которой нарушается способность адекватно обрабатывать и формировать эмоции. Поскольку сон играет ключевую роль в консолидации памяти и эмоциональной регуляции, его недостаток создает дополнительную почву для развития тревожных расстройств. Социальные и когнитивные особенности также играют немаловажную роль. В связи с особенностями воспитания женщины более склонны к катастрофизации мышления и избыточному прогнозированию возможной опасности: они часто пытаются предугадать худший сценарий, даже когда реальной угрозы нет. Такое поведение превентивно запускает стрессовый ответ, что делает женщин более уязвимыми к хроническому стрессу. Интересно, что, женщины более склонны к развитию ПТСР несмотря на то, что мужчины чаще попадают в ситуации потенциальной опасности (например, в связи с профессиональной деятельностью или склонностью к рискованному поведению). Таким образом, склонность женщин к развитию ПТСР, как и склонность к тревожным расстройствам в целом, объясняется сочетанием биологических, когнитивных и социальных факторов. Гипермнезия, гиперсенсибилизация к опасности, низкая активность ГАМК-ергической системы, перфекционизм, нарушения сна и склонность к катастрофизации мышления – все это делает женщин более уязвимыми к последствиям эмоциональной травмы.
Гендерные особенности терапии тревоги
Тревожные расстройства требуют индивидуального подхода к лечению, в том числе с учетом гендерных различий. Женщины, как уже было отмечено, более склонны к развитию тревоги и чаще сталкиваются с ее тяжелыми проявлениями. Поэтому важно учитывать особенности их физиологии и психологии при выборе методов терапии. Одним из ключевых направлений в лечении тревожных расстройств является использование анксиолитиков, однако их применение имеет свои нюансы, которые необходимо учитывать.
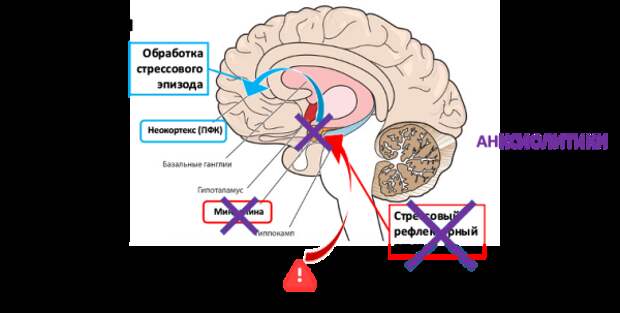
Миндалина, являющаяся центральной структурой в формировании тревожных реакций, регулируется активностью ГАМК-ергической системы. Классические анксиолитики, такие как бензодиазепины, действуют как агонисты ГАМК-ергических рецепторов, за счет чего они эффективно тормозят гиперактивацию миндалины и обеспечивают быстрый и выраженный противотревожный эффект (Рис. 4). Это особенно важно на начальных этапах терапии, когда необходимо быстро купировать острые симптомы тревоги. Однако, несмотря на свою эффективность, прием бензодиазепинов часто связан с рядом серьезных побочных эффектов. К ним относятся привыкание, заторможенность, ухудшение когнитивных функций, провокация слабости и усиление астении. Эти ограничения делают бензодиазепины менее предпочтительными для длительного применения, особенно у пожилых пациентов, у которых препараты могут вызывать кардиоваскулярные осложнения, провоцировать когнитивные расстройства и увеличивать риск падений. В связи с высоким риском развития нежелательных реакций, использование бензодиазепинов требует постоянного контроля и специализированного наблюдения.
Рисунок 4. Терапевтические мишени анксиолитической терапии.
В связи с ограничениями «классических» анксиолитиков особый интерес представляет тофизопам (Грандаксин) – препарат, который сопоставим по эффективности с бензодиазепинами, но при этом лишен многих их побочных эффектов. Он не вызывает седативного действия, не ухудшает когнитивные процессы и не вызывает привыкания и седации. В то время как «классические» бензодиазепины связываются с ω-1 сайтами ГАМК-БЗД комплекса рецепторов ГАМК, обуславливающими антиконвульсивный, миорелаксационный и седативный эффекты, тофизопам, как «неклассический» бензодиазепин, действует на ω-2 сайты, проявляя анксиоселективный эффект.
При длительном лечении рекомендуемая суточная доза тофизопама составляет от 50 до 300 мг или 1-2 таблетка от 1 до 3 раз в день. В случае нерегулярного использования препарат применяется разово по 1-2 таблетки. Максимальная суточная доза тофизопама не должна превышать 300 мг. При необходимости совместно с Грандаксином могут назначаться снотворные средства, однако следует помнить, что при совместном применении тофизопам может усиливать эффекты препаратов, угнетающих центральную нервную систему. Назначение психокорректоров в субтерапевтических дозах может снижать эффективность тофизопама и повышать риск прогрессирования заболевания. В целом, препарат хорошо переносится и во время его приема обычно не наблюдается уменьшение активности и психического бодрствования, поэтому постепенное повышение дозы обычно не требуется, и лечение можно начинать сразу с необходимой дозировки [6].
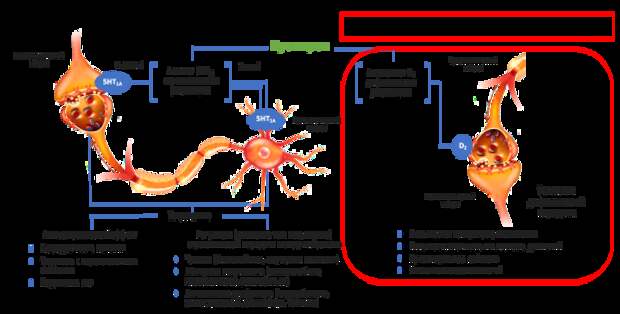
Буспирон (Спитомин) является атипичным анксиолитиком, который может назначаться для лечения ГТР, а также в комплексной терапии тревоги и депрессии, наряду с тофизопамом. Буспирон действует как частичный агонист 5НТ1А постсинаптических и полный агонист 5НТ1А пресинаптических серотониновых рецепторов. Это положительно влияет на коррекцию депрессии, трудностей с переключением внимания и нарушений сна. Помимо этого, регуляция серотониновой передачи способствует снижению непосредственно тревоги, вегетативной дисфункции, а также моторного напряжения, которое часто проявляются головными болями и невозможностью расслабиться. Наконец, действие буспирона на пресинаптические D2 дофаминовые рецепторы приводит к активации системы вознаграждения – важнейшего «источника» тревоги в мозге женщины. Усиление дофаминовой передачи, в свою очередь, способствует улучшению концентрации внимания, а также нормализации сексуальных и двигательных функций (Рис. 5).
Рисунок 5. Механизм действия и эффекты буспирона (Спитомин).
В 2024 и в 2025 гг. буспирон был включен в Федеральные клинические рекомендации в качестве средства терапии генерализованного тревожного расстройства, тревожно-фобических расстройств у взрослых, ПТСР, специфических расстройств личности, депрессивного эпизода, рекуррентного депрессивного расстройства, а также ишемического инсульта и транзиторной ишемической атаки у взрослых [7–9]. Спитомин является первым препаратом буспирона в России [10]. Одна таблетка Спитомина содержит 10 мг активного вещества, а в одной упаковке содержится 60 таблеток. Рекомендуемая начальная доза составляет 15 мг, обычная суточная доза – 20-30 мг, а максимальная суточная доза – 60 мг. Терапевтический эффект развивается постепенно и отмечается через 7-14 дней от начала лечения [9,10].
Учитывая, что женщины более склонны к тревожным расстройствам и часто сталкиваются с их длительным и тяжелым течением, выбор препаратов анксиолитической терапии должен опираться на знания о биологических и психофизиологических особенностях организма женщины. Женщины также чаще, чем мужчины, испытывают побочные эффекты от лекарств, включая седацию и когнитивные нарушения. Поэтому такие препараты, как тофизопам, могут стать оптимальным выбором для женщин, позволяя снижать тревожность без ущерба для качества жизни. Кроме того, важно учитывать, что женщины чаще страдают от сопутствующих расстройств, таких как депрессия или бессонница, что требует комплексного подхода к терапии. В таких случаях анксиолитиком выбора может стать буспирон, который можно комбинировать с другими препаратами, например, антидепрессантами или снотворными, но только под строгим контролем врача.
Таким образом, терапия тревожных расстройств у женщин требует особого внимания к выбору препаратов и методов лечения. Учет гендерных особенностей при лечении тревоги не только повышает эффективность терапии, но и помогает улучшить качество жизни пациенток, минимизируя риски побочных эффектов. Классические анксиолитики, такие как бензодиазепины, хотя и проявляют быстрый и выраженный эффект, имеют ряд ограничений, особенно для длительного применения. Тофизопам и буспирон –анксиолитики с благоприятным профилем безопасности и высокой анксиоселективностью. Тофизопам снижает тревожность без седации, а буспирон, воздействуя на серотониновые и дофаминовые рецепторы, способствует коррекции апатии, нарушений сна и вегетативной дисфункции. Комплексный подход с учетом сопутствующих расстройств и внимательный контроль врача позволяют повысить эффективность лечения и качество жизни пациенток.
Список литературы
- McLean CP, Asnaani A, Litz BT, Hofmann SG. Gender differences in anxiety disorders: prevalence, course of illness, comorbidity and burden of illness. J Psychiatr Res. 2011;45(8):1027-35.
- Li S, Jia Z, Zhang Z, Li Y, Ding Y, Qin Z, Guo S. Effect of gender on the association between cumulative cardiovascular risk factors and depression: results from the US National Health and Nutrition Examination Survey. Gen Psychiatr. 2023;36(4):e101063.
- Vesga-López O, Schneier FR, Wang S, Heimberg RG, Liu SM, Hasin DS, Blanco C. Gender differences in generalized anxiety disorder: results from the National Epidemiologic Survey on Alcohol and Related Conditions (NESARC). J Clin Psychiatry. 2008;69(10):1606-16.
- Mochcovitch MD, da Rocha Freire RC, Garcia RF, Nardi AE. A systematic review of fMRI studies in generalized anxiety disorder: evaluating its neural and cognitive basis. J Affect Disord. 2014;167:336-42.
- Domonkos E, Hodosy J, Ostatníková D, Celec P. On the Role of Testosterone in Anxiety-Like Behavior Across Life in Experimental Rodents. Front Endocrinol (Lausanne). 2018;9:441.
- Инструкция по медицинскому применению препарата Грандаксин®.
- Flavio Guzman [электронный ресурс] URL: http://psychopharmacologyinstitute.com/cns-receptors/5-ht1a-receptors/.
- Быков Ю.В., Беккер Р.А. Буспирон в практике врача-психиатра: только ли анксиолитик? Психиатрия и психофармакотерапия. 2017;19(5):32–52.
- Инструкция по медицинскому применению ЛП Спитомин (таблетки), РУ П N013159/01
- ГРЛС [электронный ресурс] URL: https://inlnk.ru/O1MM4x.
Свежие комментарии