На нашем портале мы достаточно часто пишем о попытках понять и обуздать болезнь Альцгеймера. Не менее часто мы пишем о глиальных клетках, которые в последние полтора десятилетия стали новым фокусом исследований в нейронауках. И регулярно мы рассказываем об атласах мозга. В новой статье, вышедшей в журнале Nature Neuroscience, сошлись все три тематики. Исследователи из США и Германии, используя современные омиксные технологии, проследили судьбу различных субпопуляций астроцитов в разных участках головного мозга на разных стадиях болезни Альцгеймера.
«Наша статья появилась в результате растущего осознания того, что, хотя нейроны традиционно были на переднем крае исследований болезни Альцгеймера, другие важнейшие клетки мозга, такие как астроциты, оставались недостаточно изученными в этом контексте, — говорит Судешна Дас, ведущий автор исследования, — Астроциты играют жизненно важную роль в поддержании здоровья и функций мозга, однако их участие в развитии болезни Альцгеймера изучено относительно недостаточно. Воспользовавшись недавними достижениями в омиксных технологиях, которые значительно расширили наше понимание молекулярных путей, мы стремились глубже изучить роль «астроцитов-неудачников» в развитии заболевания».
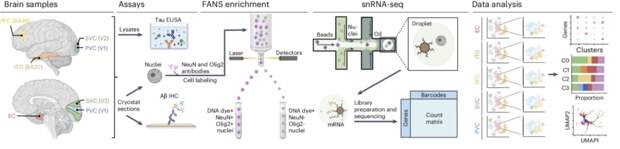
Графическое представления дизайна исследования
В исследовании авторы использовали методику секвенирования РНК из одного клеточного ядра (single-nucleus RNA sequencing, snRNA study) 628 943 астроцитов из пяти регионов мозга, взятых у 32 доноров с разными состояниями – от нормального старения до тяжелой формы болезни Альцгеймера.
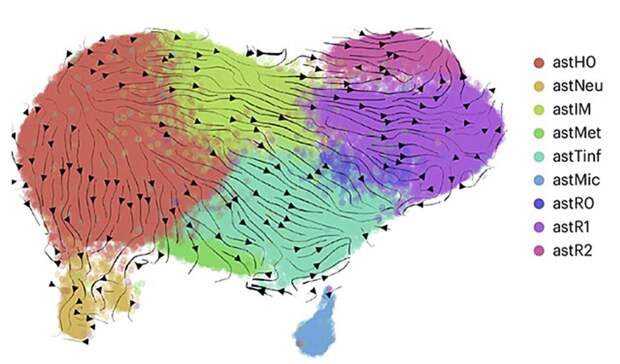
Исследователям удалось выделить несколько уникальных субкластеров астроцитов, которые по-разному реагировали на заболевание в зависимости от уязвимой к «Альцгеймеру» нейронной сети (пространственная ось) или стадии прогрессирования заболевания (временная ось).
«Мы идентифицировали различные субпопуляции астроцитов, демонстрирующие различные реакции в зависимости от области мозга и стадии заболевания, — сказала Дас. – Количество «гомеостатических» астроцитов, которые поддерживают синаптическую функцию мозга, уменьшилось в регионах с развитой патологией, тогда как содержание «реактивных» астроцитов, связанных с заболеванием, пропорционально увеличилиось».
Дас и ее коллеги также выявили новые «промежуточные» состояния астроцитов, которые, по-видимому, являются переходной формой между «гомеостатической» и «реактивной» формами астроцитов. Оказалось, что эти промежуточные состояния сильно различаются в разных областях мозга и на разных стадиях БА.
Как пишут авторы, соотношение гомеостатических, промежуточных и реактивных астроцитов изменялось только вдоль пространственной оси, в то время как два других подкластера изменялись вдоль временной оси. Количество астроцитов из одного из них, подкластера, богатого трофическими факторами, снижалось во время прогрессирования заболевания, в то время как количество астроцитов из другого (названного авторами «выгоревшей» популяцией) увеличивалось на поздней стадии, но возвращалоськ исходному уровню на конечной стадии, что указывает на истощение реакции при хроническом воздействии невропатологии.
Авторы подчеркивают, что их исследование подчеркивает сложную динамику астроцитарных реакций при болезни Альцгеймера. В будущем это может привести к новым исследованиям с упором на астроциты и другие глиальные клетки, что потенциально послужит основой для разработки принципиально новых терапевтических подходов.
«Вместе с нашими коллегами из AbbVie Inc мы также изучали прогрессирование микроглии, эндотелия и нейрональных клеток при БА, — добавила Дас. — Нашим следующим шагом будет понимание того, как эти клетки взаимодействуют с другими, вызывая нейродегенерацию при болезни Альцгеймера. С этой целью мы будем использовать пространственную транскриптомику для картирования паттернов экспрессии генов этих клеток in situ в ткани мозга».
Текст: Алексей Паевский
Serrano-Pozo, A., Li, H., Li, Z. et al. Astrocyte transcriptomic changes along the spatiotemporal progression of Alzheimer’s disease. Nat Neurosci 27, 2384–2400 (2024). https://doi.org/10.1038/s41593-024-01791-4
Свежие комментарии